今回はサリドマイドの話をしていきたいと思います。
動画版はこちら↓
薬害とは?
薬を使用する上で副作用は避けられないものです。副作用は時に取り返しのつかない健康被害をもたらしたり、命に係わる副作用が発現する場合もあります。
しかし、薬害というものはそれとは明確に異なる性質を持つものです。
薬害とは、様々定義されていますが、特に不適切な医療行為や行政の関与が示唆されるものを非難する際に使用されることが多い単語です。一般的には「医薬品の有害性に関する情報を、加害者側が(故意にせよ過失にせよ)軽視・無視した結果、社会的に引き起こされる人災的な健康被害」という認識がされているようです。様々定義は存在していますが、これらに共通するのは「医薬品自体の問題」というよりは、医薬品の使用方法に問題があるという点です。
薬害は非常に不幸な例ではありますが、これをきっかけに安全性評価方法の改善、システムの改良がなされてきました。
サリドマイドとは?
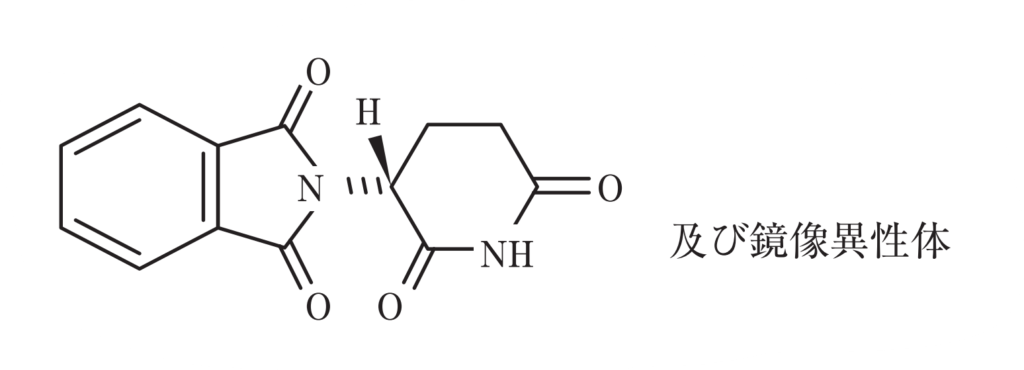
サリドマイドは1950年代に開発された催眠剤です。
米国を除く世界各国で発売され、日本では睡眠薬「イソミン」(1958年)、胃腸薬「プロバンM」(1960年)として発売されました。
しかし、1960年代初頭に「胎児に重い先天性異常を引き起こす」ということが明らかになり、販売中止になりました。
サリドマイドの歴史
1952年にチバ製薬によって最初に合成されましたが、この時「薬理作用はない」として開発は中止されました。それを西ドイツのグリュネンタール社が買収し、1958年にヒトのてんかん治療薬として販売されました。しかし、それについては大きな効果はなかったようです。そしてここで、「睡眠を誘発する作用がある」ということが判明しました。
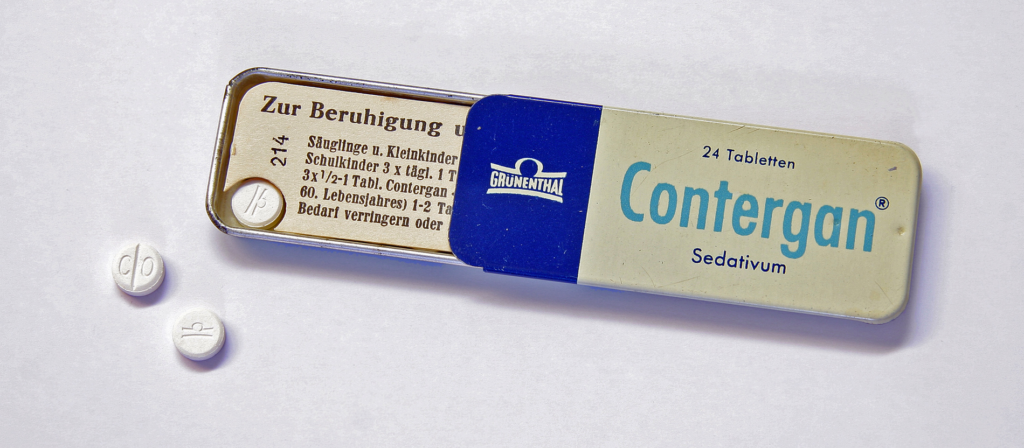
その睡眠をもたらす作用を利用して、サリドマイドを含有する「コンテルガン」という睡眠薬を販売しました。この時、グリュネンタール社では薬物動態試験はなされておらず、動物実験は一応なされてはいたものの、十分な慢性毒性試験・催奇形性試験は行われていない状態でした。
そしてコンテルガンは、入手に処方箋は必要なく、安く効果的な薬として知られていたため、1959年には最も人気のある睡眠薬になりました。
サリドマイドの特徴として、「即効性」「朝の持ち越し効果が少ない」「呼吸抑制作用が弱い」という点が挙げられます。この時点で使用されていた睡眠剤はバルビツール酸系睡眠薬が主流でした。これらの薬剤は「依存性」や「呼吸抑制作用が強力で、自殺目的のODがなされる」など問題を抱えていました。それらの問題がないサリドマイドは非常に良い薬であると認識されていたようです。
しかし、サリドマイド製剤の使用が増えるにつれて、次第に副作用が明らかになり始めました。
1960年にこれまでほとんど見られなかった「四肢の先天性奇形」が報告されるようになりました。しかし、これらの報告はサリドマイドとの関連が見出されなかったため、あまり注目されることはありませんでした。1961年に入るとさらに多くの症例報告が上がり、これによってサリドマイドに何かしら有害な作用があるのではないか?と注意が払われるようになりました。
そして、1961年11月20日、小児科医で遺伝学者でもあった西ドイツのレンツ博士が、デュッセルドルフの小児科学会でサリドマイドと四肢の奇形をもって生まれた子どもたちの関連を発表し、サリドマイドへの注意喚起を行いました。これは世界で初めてサリドマイドの危険性を訴えたもので、「レンツ警告」と呼ばれます。11月26日に西ドイツの新聞にサリドマイド製剤に奇形の疑惑があると報道され、その直後、グリュネンタール社はヨーロッパ各地のサリドマイドの自主回収を決定しました。
日本でのサリドマイド
日本でのサリドマイドは1957年、大日本製薬が独自製法で製造し、厚生労働省から特許を出願しています。この当時、欧米は物質に対して特許を取得する「物質特許主義」であったのにもかかわらず、日本は製造特許主義を取っていました。そのため、「同じ物質であっても製造方法が異なるため、別の物質として特許を主張できる」という方針を取っていました。そのため、当然グリュネンタール社とは法的な争いが発生しています。日本の製造特許主義が物質特許主義に変化するのは1976年のことです。

そして、大日本製薬は1958年1月にサリドマイドを含有する「イソミン」を睡眠薬として販売を開始しました。その後、1960年8月にサリドマイドを含有する胃腸薬である「プロバンM」の発売を開始しました。
1961年、グリュネンタール社から大日本製薬へサリドマイド剤の危険性が勧告されました。それを受けて1961年12月、厚生労働省と大日本製薬との協議がなされましたが、「有用な医薬品を回収すれば社会不安が生じる」として販売を続けました。
レンツ警告の後、1962年1月に大日本製薬から西ドイツに社員が派遣されましたが、レンツ博士や学者に会うことはなく、グリュネンタール社の関係者に面会したのみであったようです。それにもかかわらず、「レンツ警告には科学的根拠がない」と報告したようです。レンツ警告はレンツ博士が自身で疫学調査をし、自身で統計処理を行い、その結果から警告を発したものであるため、そのメカニズムについては解明されていませんでした。
「日本でサリドマイド禍が発生している」ということを最初に報告したのは梶井正博士と言われています。梶井博士は症例を7つ、イギリスの医学雑誌である「The Lancet」へ投稿しました。その後、国内の学会で同じ内容を発表し、それを報道したのが読売新聞の「日本にも睡眠薬の脅威」という記事です。
この報道によってそれまで日本で注視されていなかったこの問題が大きく注目を集め、1962年9月に販売停止、自主回収が発表されました。これは西ドイツで自主回収が行われてから10か月ほど遅れた対応でした。レンツ警告が発されてから1962年9月まで、サリドマイド剤は睡眠薬、胃腸薬として使用され続けたため、被害は広まり続けたことになります。
レンツ警告に対する対応に対しては大きくその方針が変更されました。サリドマイド禍では、科学的根拠がないと判断したために対応が遅れました。確定的な被害が出てからの対応では遅いくなってしまうため、疑わしいものを規制することを徹底することとしました。そのほかにも多くの部分で変更が起こり、現代に至ります。
サリドマイドはなぜ催奇形性を持つのか?
サリドマイド剤は1961年のレンツ警告によって催奇形性が指摘されていましたが、この機序は長らく不明でした。2010年にサリドマイドが標的としている分子が特定され、その機序が徐々に解明されています。
簡単に機序を紹介します。
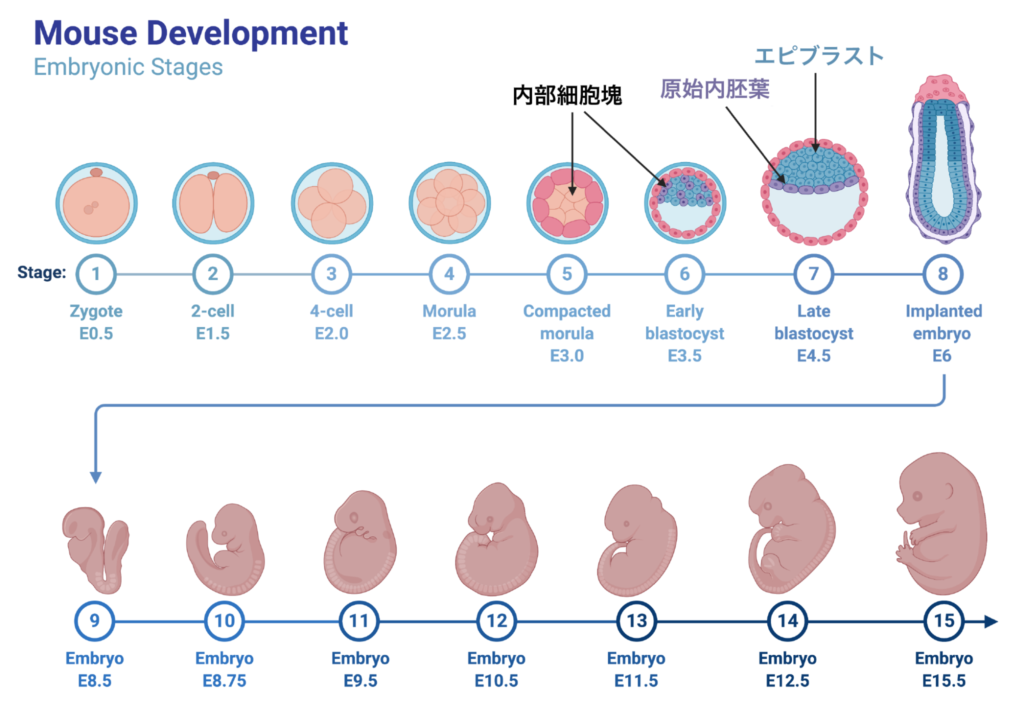
こちらはマウスの発生を示した図です。
最初はただ一つの細胞からなる受精卵で、それが分裂を繰り返すことで体を作り出します。
しかし、発生の過程では、ただ一つの受精卵が体を構成する「特定の機能に特化した細胞」細胞へ変化する必要があります。この過程を「分化」と言います。分化は厳重に制御されており、特定のタイミングで起こるように調整されています。分化を引き起こすトリガーとなるのは特定の物質であり、これらが協調して作用することで体を構築していきます。
サリドマイドはその特定のタンパク質を分解するという作用を持っており、これにより分化を妨害するために先天性奇形が発生したと考えられています。
サリドマイドのその後
1965年、イスラエルの医師によってハンセン病の2型らい反応を示した患者に「鎮痛薬」として投与された結果、その症状が治癒したことが報告されました。その後、様々な臨床試験を行った結果、その有効性が確認され、1998年にアメリカでハンセン病の2型らい反応に対する治療薬として承認されました。有効例では就寝前に服用し、翌朝には症状が軽快するという報告があるほどです。
非常に効果的な薬ではありますが、重大な副作用も認められるため、その使用は十分な注意をもって適正に行われる必要があります。
そして、1999年に「多発性骨髄腫に対しても有効である」ということが報告され、日本では2008年に多発性骨髄腫に対して保険適応の承認を受けています。
現在は世界50国以上で承認を受けている薬となりました。

参考文献
https://web.archive.org/web/20141009110927/https://www.rpharms.com/museum-pdfs/e3a-thalidomide-and-its-aftermath-2011.pdf
https://yakugai.akimasa21.net/thalidomide-outline/#toc_id_3_1
https://www.mhlw.go.jp/stf2/shingi2/2r9852000000rwbu-att/2r9852000000rwjr.pdf



コメント